- Услуги
- Цена и срок
- О компании
- Контакты
- Способы оплаты
- Гарантии
- Отзывы
- Вакансии
- Блог
- Справочник
- Заказать консультацию
Заказать консультацию
Пожароопасные свойства веществ
На пожарах горят обычно органические вещества, основными составными частями которых в подавляющем большинстве являются углерод, водород и кислород. При сгорании органических веществ выделяются токсичные газы и другие побочные продукты, которые в значительной степени изменяют процентное количество газов, входящих в атмосферный воздух, и которые по-разному воздействуют на человека (фосген, окислы азота, монооксиды углерода и т.д.).
Далее рассмотрены свойства газов, как входящих в состав атмосферного воздуха, так и образующихся при горении веществ.
Азот — бесцветный газ, не имеющий запаха, малорастворим в воде* немного легче воздуха (1,25 г/л). Азот не горит и не поддерживает горения. В обычных условиях газ физиологически безвреден, нейтрален, но с увеличением парциального давления (р >!0,55 МПа) начинает оказывать токсическое действие.
Кислород — газ, необходимый для жизни человека. При дыхании он соединяется в легких с гемоглобином крови и разносится по всем клеткам и тканям организма, где потребляется в процессе окисления. Это бесцветный газ, не имеющий запаха. Он немного тяжелее воздуха (1,43 г/л), не горит, но хорошо поддерживает горение.
В больших концентрациях даже в условиях атмосферного давления кислород действует на организм человека отравляюще. Например, при р – 0,1 МПа (1 кгс/см2) дыхание чистым кислородом в атмосферных условиях в течение трех суток приводит к тому, что в легких человека развиваются воспалительные процессы. А при парциальном давлении кислорода более 0,3 МПа (3 кгс/см2) через 15…30 мин у человека возникают судороги, он теряет сознание. К факторам, ведущим к возникновению кислородного отравления, относятся содержание во вдыхаемом воздухе примеси углекислого газа, напряженная физическая работа, переохлаждение и перегревание.
При малом парциальном давлении кислорода во вдыхаемом воздухе (ниже 0,015 МПа (0,15 кгс/см2)) кровь, протекая через легкие, насыщается кислородом неполностью, что приводит к снижению работоспособности, а в случаях острого кислородного голодания — к потере сознания.
Углекислый газ при обычных условиях бесцветный с особым кислым вкусом. Он не горит и не поддерживает горения, примерно в 1,5 раза тяжелее воздуха, плохо растворяется в воде, в организме человека образуется как конечный продукт окислительных процессов в тканях и удаляется из организма через легкие в процессе дыхания и через кожу.
Нормальное содержание углекислого газа в организме человека поддерживается центральной нервной системой посредством регуляции деятельности сердечно-сосудистой и дыхательной систем. При увеличении содержания СО2 во вдыхаемом воздухе в организме человека накапливается большое его количество. При содержании углекислого газа во вдыхаемой газовой смеси до 3 % обычно учащается сердцебиение и увеличиваются частота и глубина дыхания. Эти физиологические реакции направлены на удаление из организма избыточного содержания углекислого газа. При содержании СО2 во вдыхаемой газовой смеси более 3 % и длительном воздействии в организме возникают патологические из
менения в центральной нервной системе, сердечно-сосудистой и дыхательной системах, а также нарушение обменных процессов.
Повышенное давление углекислого газа усиливает токсическое действие кислорода и наркотическое действие азота. При нормальном атмосферном давлении в организме человека массой 70 кг растворен 1 л азота.
Количество газа, которое может раствориться в крови, зависит от величины парциального давления, времени пребывания под давлением, а также от скорости кровотока и объема легочной вентиляции. При повышении физической нагрузки скорость кровотока увеличивается, поэтому насыщение организма газами увеличивается.
Снижение давления (декомпрессия) вызывает освобождение организма от азота. Избыток растворенного газа при этом попадает из тканей в кровяное русло и током крови выносится в легкие, откуда удаляется в окружающую среду.
При быстром снижении давления растворенный в тканях газ начинает образовывать пузырьки различной величины. Током крови они могут разноситься по всему телу и вызывать закупорку кровеносных сосудов, что приводит к декомпрессионной (кессонной) болезни.
Наряду с углекислым газом в продуктах горения, образующихся на пожарах, выделяется оксид углерода.
Оксид углерода — газ, не имеющий цвета и запаха, намного легче воздуха (1,25 г/л), почти не растворяется в воде, хорошо горит.
Токсичное (отравляющее) действие СО основано на том, что этот газ активно соединяется с гемоглобином крови, образуя нестойкое соединение карбоксигемоглобин. В этом случае организм человека испытывает острый недостаток кислорода.
Степень тяжести отравления оксидом углерода в основном зависит от концентрации его во вдыхаемом воздухе, продолжительности воздействия и интенсивности легочной вентиляции.
Строительные материалы могут быть разделены на четыре класса по степени воздействия на человека продуктов горения:
- чрезвычайно опасные (регламентирующее значение — 1г) —виларес, слоистый трудносгораемый пластик;
- высокоопасные (1…3 г) — пенополиуретан ППУ-306, слоистый декоративный пластик, древесина лиственницы, полиамидные материалы и пленки, полиэтилентерефталатная пленка;
- опасные (3…9 г) — пластмасса ЛКФ-2, линолеум ТТН, эпоксидный стеклопластик, теплоизоляционные плиты ФС, пленка ПТГМ-609, теплозвукоизоляционная композиция АТМ-1;
- малоопасные (9 г) — полиэфирный стеклопластик, пентофталевая эмаль ПФ-218, мастичное покрытие «Нева ЗУ».
Следовательно, к классу чрезвычайно опасных материалов отнесены виларес и слоистый трудносгораемый пластик. Первый характеризуется высоким уровнем выделения окиси углерода, второй кроме оксида углерода выделяет чрезвычайно токсичное соединение — цианистый водород.
Цианистый водород выделяют и другие пластмассы на основе азота (полиакрилонитрил, полиамиды, полиуретаны).
Класс высокоопасных материалов включает в себя изделия из древесины (фанера, древесина, лиственница), что свидетельствует о том, что материалы из древесины по токсичности продуктов горения превосходят многие синтетические материалы.
Малоопасные по токсичности материалы характеризуются низким уровнем выделения летучих веществ и большим зольным остатком.
Горение — это сложное, быстро протекающее химическое превращение веществ, сопровождающееся выделением теплоты и излучением света. В большинстве случаев горение происходит в результате взаимодействия горючего вещества с окислителем (кислородом воздуха, хлором, закисью азота и др.) при наличии источника зажигания.
При определении пожаровзрывоопасности веществ и материалов различают:
- газы — вещества, давление насыщенных паров которых при температуре 25 °С и давлении 101,3 кПа превышает 101,3 кПа;
- жидкости — вещества, давление насыщенных паров которых при температуре 25 °С и давлении 101,3 кПа меньше 101,3 кПа. К жидкостям относятся также твердые плавящиеся вещества, температура плавления или каплепадения которых меньше 50 °С;
- твердые вещества и материалы — индивидуальные вещества и их смесевые композиции с температурой плавления или каплепадения больше 50 “С, а также вещества, не имеющие температуру плавления (например, древесина, ткани и др.);
- пыли — диспергированные твердые вещества и материалы с размером частиц менее 850 мкм.
В зависимости от агрегатного состояния (твердое, жидкое, газообразное) горючего вещества и окислителя различают три вида горения: гомогенное — горение газов и парообразных горючих веществ в среде газообразного окислителя; гетерогенное — горение жидких и твердых горючих веществ в среде газообразного окислителя; горение взрывчатых веществ и порохов .
По скорости распространения пламени горение подразделяют на три вида: .
- дефлаграционное, когда скорость горения составляет несколько метров в секунду;
- взрывное — десятки метров в секунду;
- детонационное — тысячи метров в секунду.
Большинству пожаров свойственно дефлаграционное горение. Равномерное распространение горения устойчиво лишь в том случае, если оно сопровождается повышением давления. Когда горение происходит в замкнутом пространстве или выход газообразных продуктов сгорания затруднителен, то повышение температуры приводит к интенсивному расширению газовых объемов и взрыву.
Возможен также механизм распространения горения, связанный с ударными волнами. Ударная волна вызывает при своем прохождении нагревание газа, и повышение его температуры может оказаться достаточным для возникновения процесса горения. При своем движении ударная волна как бы поджигает горючую смесь, т. е. горение распространяется со скоростью, равной скорости волны.Причем, выделяющаяся при этом химическая энергия подпитывает ударную волну и не дает ей затухать. Такой механизм распространения горения называют детонацией. Поведение образовавшейся детонационной волны и ее разрушающее действие не зависят от того, движется она в открытом или замкнутом объеме. Это обстоятельство влияет на возникновение волны, для которого необходим преддетонационный разгон пламени — расстояние от точки зажигания до места возникновения детонационного горения. Поэтому горение газообразных сред в емкостях редко переходит в детонацию и в основном проявляется в трубах.
Для возникновения горения жидкости необходимо образование горючей паровоздушной смеси около ее поверхности. Внесение источника зажигания приводит к воспламенению или вспышке паровоздушной смеси. При устранении источника зажигания в зависимости от сложившихся условий может произойти либо прекращение процесса горения, либо его распространение.
Таким образом, горение жидкостей представляет собой гомогенный химический процесс горения паров этих жидкостей в кислородной среде. Интенсивность процесса горения определяется скоростью испарения, зависящей от подводимой к жидкости теплоты.
При анализе горения твердых веществ выделяют две основные стадии процесса.
Первая стадия процесса связана с тем, что любое твердое горючее вещество содержит компоненты, которые при нагреве разлагаются и образуют летучую паровоздушную смесь, горение которой полностью соответствует гомогенной газофазной химической реакции.
После окончания выхода летучих компонентов начинается вторая стадия процесса, для которой характерно взаимодействие между веществами, находящимися в разных агрегатных состояниях (твердое горючее вещество и газообразный окислитель). Реакции такого типа называются гетерогенными, а процесс горения — гетерогенным.
Необходимо отметить, что при нагреве пылевидных горючих частиц, который происходит очень быстро, образование летучих фракций затягивается и продолжается в процессе гетерогенного горения.
Горючесть — способность вещества или материала к горению. По горючести все вещества и материалы подразделяются на три группы:
- негорючие (несгораемые) — вещества и материалы, неспособные к горению в воздухе (материалы минерального происхождения и изготовленные на их основе — красный кирпич, силикатный кирпич, бетон, камень, асбест, асбоцемент, минеральная вата, большинство металлов и др.). При этом негорючие вещества могут быть пожароопасными, например вещества, выделяющие горючие продукты при взаимодействии с водой, кислородом воздуха или друг с другом;
- трудногорючие (трудносгораемые) — вещества и материалы,способные возгораться в воздухе от источника зажигания, но не способные самостоятельно гореть после его удаления (материалы, содержащие сгораемые компоненты, например древесина при глубокой пропитке антипиренами, фибролит и т.д.);
- горючие (сгораемые) — вещества и материалы, способные самовозгораться, а также возгораться от источника зажигания и самостоятельно гореть после его удаления.
Из группы горючих веществ и материалов выделяют легковоспламеняющиеся вещества и материалы.
Легковоспламеняющимися называют горючие вещества и материалы, способные воспламеняться от кратковременного (до 30 °С) воздействия источника зажигания с низкой энергией (пламя спички, искра, тлеющая сигарета и т.д.).
Вспышка — быстрое сгорание горючей смеси, не сопровождающееся образованием сжатых газов.
Для более полного представления процесса вспышки введено понятие температура вспышки — это самая низкая температура горючего вещества, при которой в условиях специальных испытаний над его поверхностью образуются пары или газы, способные вспыхивать от источника зажигания, но скорость их образования еще не достаточна для устойчивого горения.
Этот показатель служит для оценки пожаровзрывоопасности в основном горючих жидкостей, однако некоторые твердые вещества (нафталин, фосфор, камфора и т.д.), заметно испаряющиеся при нагреве, также могут оцениваться этим показателем.
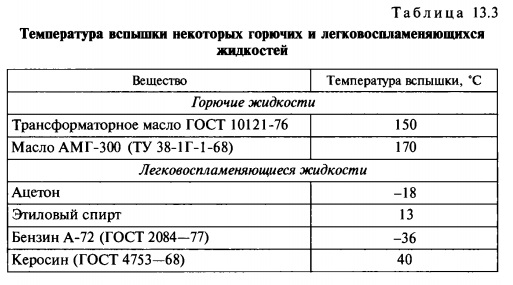
Экспериментальное определение температуры вспышки жидкости проводят нагреванием определенного количества ее с заданной скоростью; при этом периодически поднимают, визуально регистрируя, результат зажигания. Экспериментальное определение температуры проводят как для открытых, так и для закрытых тиглей. Для однокомпонентных веществ температура вспышки постоянна, в то время как для сложных веществ она зависит от состава и свойств компонентов. В табл. 13.3 приведены значения температуры вспышки некоторых горючих и легковоспламеняющихся жидкостей.
Легковоспламеняющимися называются жидкости с температурой вспышки не более 61 °С в закрытом тигле или 66 °С в открытом тигле.
Не менее важным показателем, характеризующим процесс горения, является температура воспламенения — наименьшая температура вещества, при которой в условиях специальных испытаний вещество выделяет горючие пары и газы с такой скоростью, что после их зажигания возникает устойчивое пламенное горение.
При достижении температуры самовоспламенения происходит резкое увеличение скорости экзотермических реакций, заканчивающихся пламенным горением. Экспериментальное определение этого показателя пожароопасности заключается в измерении минимальной температуры равномерно прогретого объема исследуемой горючей смеси, при которой происходит самовоспламенение этого объема в отсутствии источника зажигания.
Температура самовоспламенения вещества меняется в зависимости от концентрации, давления, размеров, формы.
Вещества с высокой температурой самовоспламенения горят только в результате нагрева.
Вещества с температурой самовоспламенения, находящейся в пределах температуры окружающей среды, могут самовоспламеняться без нагрева, так как окружающая среда нагревает их до температуры самовоспламенения. Такие вещества представляют большую пожарную опасность и называются самовозгорающимися, а процесс самонагревания их до возникновения горения —самовозгоранием.
Самовозгорающиеся вещества способны гореть и взрываться при взаимодействии с водой, кислородом воздуха и другими веществами. Они представляют большую пожароопасность. К ним относятся бурые и каменные угли, торф, серный колчедан, щелочные металлы и др.
Многообразие веществ и материалов предопределило различные концентрационные пределы распространения пламени. Существуют такие понятия, как нижний и верхний концентрационные пределы распространения пламени (воспламенения) — это соответственно минимальное и максимальное содержание горючего в смеси горючее вещество—окислительная среда, при котором возможно распространение пламени по смеси на любое расстояние от источника зажигания.
Интервал концентраций между нижним и верхним пределами называется областью распространения пламени (воспламенения).
Методы экспериментального и расчетного определения концентрационных пределов распространения пламени тестированы (ГОСТ 12.1.044—85 «Пожаровзрывоопасность веществ и материалов. Номенклатура показателей и методы их определения»).
Пределы распространения пламени горючих смесей непостоянны и зависят:
- от начальной температуры. Если температура повышается, тодиапазон взрываемости расширяется, причем нижний предел становится меньше, а верхний — больше. Принято считать, что с повышением температуры смеси на каждые 100 °С нижний предел уменьшается на 10 % от исходного значения, а верхний — возрастает на 15%. Повышение начальной температуры горючей смеси за счет снижения градиента температур приводит к уменьшению оттока из зоны горения к исходной смеси. Это увеличивает скорость горения, и, соответственно, уменьшает время теплообмена горючей системы с окружающей средой. Снижение теплопотерь в горючей системе ведет к повышению ее температуры, и поэтому разбавленная воздухом горючая смесь, не взрывающаяся при низкой температуре, становится взрывоопасной при более высокой температуре;
- давления горючей смеси. Повышение давления выше атмосферного для большинства смесей приводит к расширению области воспламенения, а уменьшение давления сужает эту область. Каждая смесь при любой концентрации и определенной температуре имеет пороговую величину давления, ниже которой взрыв невозможен;
- наличия других примесей. Добавление негорючих газов существенно снижает верхний предел распространения пламени. При этом нижний предел распространения пламени почти не изменяется, так как введение негорючей примеси незначительно влияет на концентрацию кислорода, определяющего способность смеси к взрыву. Увеличение концентрации негорючих веществ приводит или может привести к тому, что смесь становится невзрываемой. В зону горения вводят негорючие газообразные вещества — флегматизаторы;
- характера источника воспламенения (например, мощности электрического разряда). Каждой горючей смеси при определенных условиях соответствует минимальная энергия воспламенения. Эту энергию сообщают горючей смеси электрический разряд, дуга, открытое пламя или другой источник тепла. Чем выше мощность искры, тем вероятнее возникновение устойчивого горения и взрыва, шире становится диапазон взрываемости. Опасность взрыва горючей смеси возрастает, если увеличивается продолжительность искрового разряда.
Определенной температуре жидкости соответствует определенная упругость паров над поверхностью жидкости, что позволяет определить взрывоопасность горючих веществ с учетом температурных пределов воспламенения, т.е. с учетом температуры вещества, при которой его насыщенные пары образуют в конкретной окислительной среде концентрации, равные соответственно нижнему (нижний температурный предел (НП)) и верхнему (верхний температурный предел (ВП)) концентрационным пределам распространения пламени (воспламенения), %:
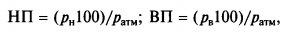
где Рн Рв — давление насыщенных паров при температурах, соответствующих нижнему и верхнему температурным пределам, Па; Ратм — атмосферное давление, равное 9,8 • 103 Па.
Значения температурных пределов воспламенения веществ используют при расчете пожаровзрывобезопасных режимов работы технологического оборудования, при оценке аварийных ситуаций, связанных с разливом горючих жидкостей, а также для расчета концентрационных пределов воспламенения.
Твердые частицы горючего вещества, находясь во взвешенном состоянии (аэрозоль), в смеси с воздухом (кислородом) могут гореть с большой скоростью или взрываться.
Статьи по теме
- Экологическая экспертиза производственных предприятий
- Построение системы мониторинга окружающей среды
- Классификация систем мониторинга окружающей среды
- Расчет СЗЗ предприятия по воздействию вредных факторов на окружающую среду
- Требования, предъявляемые к санитарно-защитным зонам
- Роль безотходных и малоотходных технологий в процессе обращения с отходами
- Переработка отходов как средство защиты окружающей среды
- Классификация, паспортизация и сертификация отходов
- Основные понятия и определения. Характеристика и свойства отходов
Полезные статьи









Узнайте цену услуг:
Узнай цену консультации
"Да забей ты на эти
дипломы и экзамены!”
(дворник Кузьмич)

